Zigapusnik (Talk | contribs) (Created page with "{{Slovenia}} <html> <head> <title>Home</title> <link rel="stylesheet" href="//2016.igem.org/Team:Slovenia/libraries/semantic-min-css?action=raw&ctype=text/cs...") |
Zigapusnik (Talk | contribs) |
||
| Line 2: | Line 2: | ||
<html> | <html> | ||
<head> | <head> | ||
| − | <title> | + | <title>Domača stran</title> |
<link rel="stylesheet" | <link rel="stylesheet" | ||
href="//2016.igem.org/Team:Slovenia/libraries/semantic-min-css?action=raw&ctype=text/css"> | href="//2016.igem.org/Team:Slovenia/libraries/semantic-min-css?action=raw&ctype=text/css"> | ||
| Line 191: | Line 191: | ||
<img class = "ui large circular image" src="//2016.igem.org/wiki/images/c/cb/T--Slovenia--igemLogo.gif"> | <img class = "ui large circular image" src="//2016.igem.org/wiki/images/c/cb/T--Slovenia--igemLogo.gif"> | ||
<p style="font-size:11px;"> | <p style="font-size:11px;"> | ||
| − | + | Simbol iGEMa smo narisali s stekleno palčko na genetsko modificirano humano celično linijo in posneli vsako črko posebej. V celice smo vnesli genske konstrukte, ki so kodirali bakterijski ionski kanalček MscS, plinske mehurčke (GvpA in GcpC) ter od kalcija odvisni cepljeni luciferazni poročevalec. | |
| − | + | ||
| − | + | ||
</p> | </p> | ||
</div> | </div> | ||
| Line 204: | Line 202: | ||
<h1 class="ui centered dividing header"><span id="intro" class = "section"> </span>Sonicell</h1> | <h1 class="ui centered dividing header"><span id="intro" class = "section"> </span>Sonicell</h1> | ||
<div class = "ui segment"> | <div class = "ui segment"> | ||
| − | <p> | + | <p>Projekt Sonicell predstavlja vznemirljive novosti v sintezni biologiji, ki se osredotočajo na hiter celični odziv na zunanje dražljaje kot so zvok, svetloba ali kemični signali. Sistem je sestavljen iz dela za povečano občutljivost na ultrazvok in druge mehanične dražljaje, ki jih zaznava od kalcija odvisni poročevalec, ter dela, ki integrira več vhodnih signalov v signalno pot, ki je sestavljena iz ortogonalnih proteaz. Prenos signala je oblikovan tako, da aktivirane proteaze odcepijo signalni peptid, ki omogoča zadrževanje tarčnih proteinov v endoplazemskem retiklu. Posledica takšne cepitve je hitro izločanje proteinov iz celice.</p> |
<div> | <div> | ||
<div class = "container"> | <div class = "container"> | ||
| Line 215: | Line 213: | ||
</map> | </map> | ||
<div class="popup module1"> | <div class="popup module1"> | ||
| − | <span class="popuptext" id="module1"><b> | + | <span class="popuptext" id="module1"><b>Izboljšana občutljivost celic na mehanske dražljaje:</b><br />Občutljivost sesalskih celic na ultrazvok in druge mehanske dražljaje smo povečali z uvedbo mehanosenzitivnega ionskega kanalčka in/ali z izražanjem bekterijskih proteinskih plinskih veziklov v sesalskih celicah. Vdor kalcija skozi kanalčke zazna kompleks kalmodulina in peptida M13, kar zaznamo kot povišanje luminiscence (kar smo uporabili tudi pri risanju po celicah) ali kot sestavljanje cepljene proteaze.</span> |
</div> | </div> | ||
<div class="popup module2"> | <div class="popup module2"> | ||
| − | <span class="popuptext" id="module2"><b> | + | <span class="popuptext" id="module2"><b>Signaliziranje in procesiranje <br />informacij na osnovi proteaz:</b><br />Kombinacije proteaz s specifičnimi tarčnimi mesti cepitve omogočajo aktivacijo poročevalca ali druge proteaze, kar je osnova za oblikovanje novega tipa hitre signalne poti in tvorbo logičnih funkcij.</span> |
</div> | </div> | ||
<div class="popup module3"> | <div class="popup module3"> | ||
| − | <span class="popuptext" id="module3"><b> | + | <span class="popuptext" id="module3"><b>Izboljšana občutljivost celic na mehanske dražljaje: </b><br /> Občutljivost sesalskih celic na ultrazvok in druge mehanske dražljaje smo povečali z uvedbo mehanosenzitivnega ionskega kanalčka in/ali z izražanjem bekterijskih proteinskih plinskih veziklov v sesalskih celicah. Vdor kalcija skozi kanalčke zazna kompleks kalmodulina in peptida M13, kar zaznamo kot povišanje luminiscence (kar smo uporabili tudi pri risanju po celicah) ali kot sestavljanje cepljene proteaze.</span> |
</div> | </div> | ||
<div class="popup module4"> | <div class="popup module4"> | ||
| − | <span class="popuptext" id="module4"> <b> | + | <span class="popuptext" id="module4"> <b>S proteazami posredovano hitro <br /> izločanje terapevtskih proteinov:</b> <br />Izločanje proteina sproži proteolitična cepitev peptidne sekvence, ki omogoča zadrževanje proteina v endoplazemskem retiklu. Po odcepu sekvence se protein prenese iz endoplazemskega retikla v Golgijev aparat, kjer ga cepi naravno prisotna furinska proteaza. Sledi sproščanje proteina iz celice.</span> |
</div> | </div> | ||
</div> | </div> | ||
| Line 230: | Line 228: | ||
</div> | </div> | ||
<div class= "ui segment"> | <div class= "ui segment"> | ||
| − | <h4> | + | <h4>Povzetek</h4> |
| − | + | <p>Sintezna biologija odpira nove in vznemirljive načine nadzora nad celicami za aplikativne namene: od industrijskih procesov do celične terapije. Večina obstoječih celičnih vezij temelji na uravnavanju prepisovanja genov, kar je prepočasen postopek za večino terapevtskih ali diagnostičnih namenom, kot sta na primer dostava inzulina ali detekcija metabolitov. Zdravniki in raziskovalci, s katerimi smo se posvetovali, so poudarili pomembnost hitrega in nadzorovanega odziva, prav tako pa je močno zaželena tudi neinvazivnost pri stimulacija izbranega tkiva.</p> | |
| − | + | <p>Svetloba je uporabno orodje za hitro in prostorsko omejeno stimulacijo celic. Ultrazvok prav tako kot svetloba omogoča hiter celični odziv, hkrati pa lahko prodre globlje v tkivo. Z uvedbo bakterijskih ali sesalskih mehanosenzitivnih kanalčkov smo povečali občutljivost celic na ultrazvok. Odziv na ultrazvok in dotik smo dodatno povečali tudi z izražanjem bakterijskih proteinov GvpA in GvpC, ki tvorita stisljive plinske mehurčke. Mehanosenzitivnost smo zaznali s poročevalcem, ki je inducibilen s kalcijem. Sestavljen je iz kalmodulina, peptida M-13 in cepljene luciferaze. Ta sistem nam je omogočal risanje po celicah, kar smo izvedli v sodelovanju z umetnico iz Argentine.</p> | |
| − | + | <p>Za hiter odziv celic na več dražljajev smo oblikovali signalno pot na osnovi proteolize. Razvili smo štiri cepljene ortogonalne proteaze, vsaka izmed katerih prepozna specifično cepitveno mesto dolgo 7 aminokislinskih ostankov. Na osnovi cepitve dimerizacijske domene, ki jo sestavljata oviti vijačnici, smo dokazali uporabnost od proteolize odvisnih logičnih vrat v sesalskih celicah. S povzročitvijo proteolitične odcepitve zadrževalne sekvence s proteina vhodni signali sprožijo izločanje proteinov, s čimer se izognemo vmesnemu (počasnejšemu) koraku inducirane proteinske sinteze.</p> | |
| − | + | <p>Menimo, da smo s projektom Sonicell naredili več temeljnih premikov, ki bodo gotovo doprinesli k razvoju sintezne biologije tudi po iGEM-u ter k napredku terapevtskih, diagnostičnih in drugih aplikacij v dobrobit človeštva.</p> | |
| − | + | </div> | |
<div class = "ui segment"> | <div class = "ui segment"> | ||
| − | <h4> | + | <h4>Povzetek s preprostimi besedami</h4> |
| − | <p> | + | <p>V sintezni biologiji želimo pripraviti celice, ki bi sledile našim navodilom in počele, kar od njih potrebujemo, na primer izdelovale zdravila. V našem projektu smo celice spremenili tako, da se odzivajo na ultrazvok ali dotik. Ko se dotaknemo gojišča s takšnimi celicami, te zasvetijo, kar lahko posnamemo s fotoaparatom. Seveda želimo, da se celice na naše ukaze odzovejo karseda hitro, ker si včasih ne moremo privoščiti ene ure čakanja, preden celice izdelajo in izločijo zdravilo. Zato smo naše celice opremili z novim načinom procesiranja informacij, ki temelji na kombinaciji različnih novih encimov, ki lahko prerežejo točno določene molekule celičnih beljakovin in s tem spremenijo njihovo funkcijo. Nazadnje lahko novi encimi odrežejo tudi sidro, s katerim so zdravila pripeta v celico, ki jih je naredila, in tako povzročijo sproščanje teh zdravil v okolico. Naše celice se ne odzivajo samo na dotik in ultrazvok, temveč jim lahko s kombinacijo dotika, zvočnih, svetlobnih in kemičnih signalov dajemo različna navodila. Predstavljamo si, da bi na podoben način lahko spremenili tudi celice v možganih, da bi lahko pomagali osebam s Parkinsonovo boleznijo brez potrebe po operaciji, ali da bi sprožili hitro izločanje inzulina, kar bi pomagalo osebam z diabetesom.</p> |
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
</div> | </div> | ||
<div> | <div> | ||
| − | <h1 class="ui centered dividing header"><span id="achievements" class = "section"> </span> | + | <h1 class="ui centered dividing header"><span id="achievements" class = "section"> </span>Dosežki</h1> |
<div class = "ui segment"> | <div class = "ui segment"> | ||
<div class = "corners" style="float:right;"> | <div class = "corners" style="float:right;"> | ||
| Line 251: | Line 245: | ||
<p><img src="//2016.igem.org/wiki/images/0/0d/T--Slovenia--igemLogoSmall.png" alt="newAtiGEM" width="30" height="30" style = "display: inline;"> new at iGEM</p> | <p><img src="//2016.igem.org/wiki/images/0/0d/T--Slovenia--igemLogoSmall.png" alt="newAtiGEM" width="30" height="30" style = "display: inline;"> new at iGEM</p> | ||
</div> | </div> | ||
| − | + | <ul> | |
| − | + | <li>Z izražanjem za kalcij prepustnih kanalčkov ter s funkcionalno rekonstitucijo bakterijskih proteinskih komponent (GvpA in GvpC), ki tvorijo stisljive plinske mehurčke, smo povečali občutljivost sesalskih celic na ultrazvok in mehanske dražljaje. </li> | |
| − | + | <li>Po meri narejena naprava za generiranje ultrazvoka za stimulacijo sesalskih celic. </li> | |
| − | + | <li>V sesalskih celicah smo izrazili mehanosenzitiven senzor, ki je občutljiv na povišano koncentracijo kalcija in omogoča hitro celično reakcijo z oddajanjem svetlobe ob vzdraženju z dotikom ali ultrazvokom. Opisani senzor smo izkoristili tudi za risanje po celicah. </li> | |
| − | + | <li>Ciklično luciferazo, ki se aktivira ob proteolitični cepitvi, smo preizkusili, opisali in vključili v zbirko iGEM. </li> | |
| − | + | <li>Oblikovali smo set štirih ortogonalnih mestno specifičnih proteaz, ki smo jih preizkusili kot cepljene proteine v sesalskih celicah. </li> | |
| − | + | <li>Oblikovali smo signalno pot na osnovi ortogonalnih proteaz, ki nam hkrati omogoča procesiranje več vhodnih signalov in jo ekperimentalno preizksuili. </li> | |
| − | + | <li>Proteoliza sekvence, ki omogoča zadrževanje proteina v endoplazemskem retiklu smo uporabili za sprožitev izločanja proteinov iz celic, kar je potrebno za hitre terapevtske odzive, kot na primer sproščanje hormonov ali nevroaktivnih peptidov. </li> | |
| − | + | </ul> | |
</div> | </div> | ||
</div> | </div> | ||
Revision as of 14:48, 17 October 2016
Sonicell
Projekt Sonicell predstavlja vznemirljive novosti v sintezni biologiji, ki se osredotočajo na hiter celični odziv na zunanje dražljaje kot so zvok, svetloba ali kemični signali. Sistem je sestavljen iz dela za povečano občutljivost na ultrazvok in druge mehanične dražljaje, ki jih zaznava od kalcija odvisni poročevalec, ter dela, ki integrira več vhodnih signalov v signalno pot, ki je sestavljena iz ortogonalnih proteaz. Prenos signala je oblikovan tako, da aktivirane proteaze odcepijo signalni peptid, ki omogoča zadrževanje tarčnih proteinov v endoplazemskem retiklu. Posledica takšne cepitve je hitro izločanje proteinov iz celice.
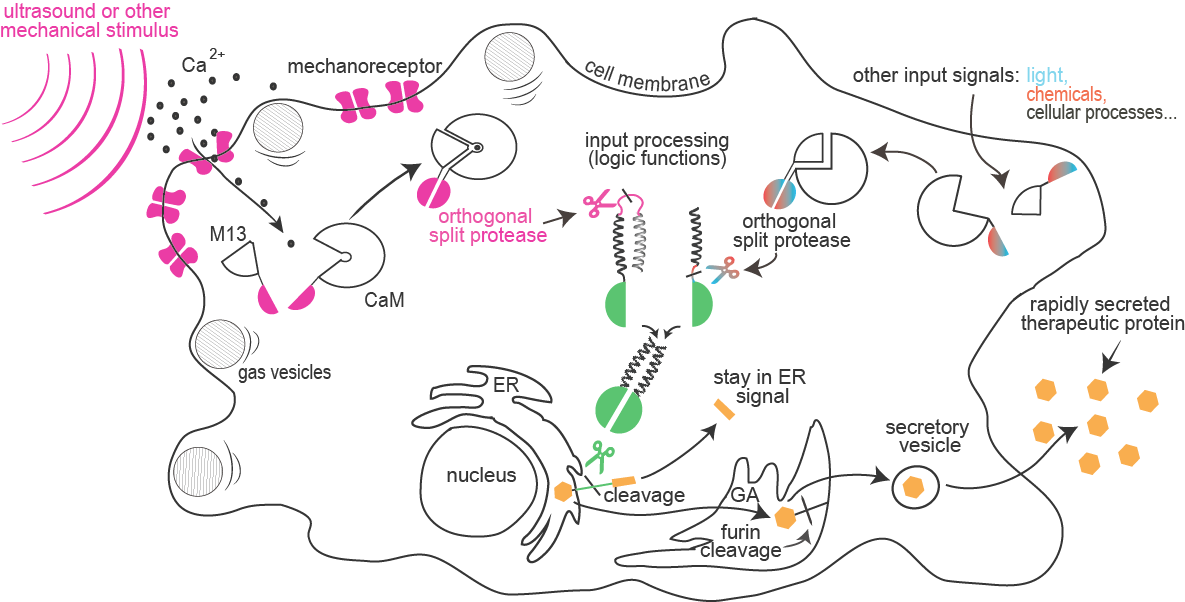
Občutljivost sesalskih celic na ultrazvok in druge mehanske dražljaje smo povečali z uvedbo mehanosenzitivnega ionskega kanalčka in/ali z izražanjem bekterijskih proteinskih plinskih veziklov v sesalskih celicah. Vdor kalcija skozi kanalčke zazna kompleks kalmodulina in peptida M13, kar zaznamo kot povišanje luminiscence (kar smo uporabili tudi pri risanju po celicah) ali kot sestavljanje cepljene proteaze.
informacij na osnovi proteaz:
Kombinacije proteaz s specifičnimi tarčnimi mesti cepitve omogočajo aktivacijo poročevalca ali druge proteaze, kar je osnova za oblikovanje novega tipa hitre signalne poti in tvorbo logičnih funkcij.
Občutljivost sesalskih celic na ultrazvok in druge mehanske dražljaje smo povečali z uvedbo mehanosenzitivnega ionskega kanalčka in/ali z izražanjem bekterijskih proteinskih plinskih veziklov v sesalskih celicah. Vdor kalcija skozi kanalčke zazna kompleks kalmodulina in peptida M13, kar zaznamo kot povišanje luminiscence (kar smo uporabili tudi pri risanju po celicah) ali kot sestavljanje cepljene proteaze.
izločanje terapevtskih proteinov:
Izločanje proteina sproži proteolitična cepitev peptidne sekvence, ki omogoča zadrževanje proteina v endoplazemskem retiklu. Po odcepu sekvence se protein prenese iz endoplazemskega retikla v Golgijev aparat, kjer ga cepi naravno prisotna furinska proteaza. Sledi sproščanje proteina iz celice.
Povzetek
Sintezna biologija odpira nove in vznemirljive načine nadzora nad celicami za aplikativne namene: od industrijskih procesov do celične terapije. Večina obstoječih celičnih vezij temelji na uravnavanju prepisovanja genov, kar je prepočasen postopek za večino terapevtskih ali diagnostičnih namenom, kot sta na primer dostava inzulina ali detekcija metabolitov. Zdravniki in raziskovalci, s katerimi smo se posvetovali, so poudarili pomembnost hitrega in nadzorovanega odziva, prav tako pa je močno zaželena tudi neinvazivnost pri stimulacija izbranega tkiva.
Svetloba je uporabno orodje za hitro in prostorsko omejeno stimulacijo celic. Ultrazvok prav tako kot svetloba omogoča hiter celični odziv, hkrati pa lahko prodre globlje v tkivo. Z uvedbo bakterijskih ali sesalskih mehanosenzitivnih kanalčkov smo povečali občutljivost celic na ultrazvok. Odziv na ultrazvok in dotik smo dodatno povečali tudi z izražanjem bakterijskih proteinov GvpA in GvpC, ki tvorita stisljive plinske mehurčke. Mehanosenzitivnost smo zaznali s poročevalcem, ki je inducibilen s kalcijem. Sestavljen je iz kalmodulina, peptida M-13 in cepljene luciferaze. Ta sistem nam je omogočal risanje po celicah, kar smo izvedli v sodelovanju z umetnico iz Argentine.
Za hiter odziv celic na več dražljajev smo oblikovali signalno pot na osnovi proteolize. Razvili smo štiri cepljene ortogonalne proteaze, vsaka izmed katerih prepozna specifično cepitveno mesto dolgo 7 aminokislinskih ostankov. Na osnovi cepitve dimerizacijske domene, ki jo sestavljata oviti vijačnici, smo dokazali uporabnost od proteolize odvisnih logičnih vrat v sesalskih celicah. S povzročitvijo proteolitične odcepitve zadrževalne sekvence s proteina vhodni signali sprožijo izločanje proteinov, s čimer se izognemo vmesnemu (počasnejšemu) koraku inducirane proteinske sinteze.
Menimo, da smo s projektom Sonicell naredili več temeljnih premikov, ki bodo gotovo doprinesli k razvoju sintezne biologije tudi po iGEM-u ter k napredku terapevtskih, diagnostičnih in drugih aplikacij v dobrobit človeštva.
Povzetek s preprostimi besedami
V sintezni biologiji želimo pripraviti celice, ki bi sledile našim navodilom in počele, kar od njih potrebujemo, na primer izdelovale zdravila. V našem projektu smo celice spremenili tako, da se odzivajo na ultrazvok ali dotik. Ko se dotaknemo gojišča s takšnimi celicami, te zasvetijo, kar lahko posnamemo s fotoaparatom. Seveda želimo, da se celice na naše ukaze odzovejo karseda hitro, ker si včasih ne moremo privoščiti ene ure čakanja, preden celice izdelajo in izločijo zdravilo. Zato smo naše celice opremili z novim načinom procesiranja informacij, ki temelji na kombinaciji različnih novih encimov, ki lahko prerežejo točno določene molekule celičnih beljakovin in s tem spremenijo njihovo funkcijo. Nazadnje lahko novi encimi odrežejo tudi sidro, s katerim so zdravila pripeta v celico, ki jih je naredila, in tako povzročijo sproščanje teh zdravil v okolico. Naše celice se ne odzivajo samo na dotik in ultrazvok, temveč jim lahko s kombinacijo dotika, zvočnih, svetlobnih in kemičnih signalov dajemo različna navodila. Predstavljamo si, da bi na podoben način lahko spremenili tudi celice v možganih, da bi lahko pomagali osebam s Parkinsonovo boleznijo brez potrebe po operaciji, ali da bi sprožili hitro izločanje inzulina, kar bi pomagalo osebam z diabetesom.
Dosežki
![]() new at science
new at science
![]() new at iGEM
new at iGEM
- Z izražanjem za kalcij prepustnih kanalčkov ter s funkcionalno rekonstitucijo bakterijskih proteinskih komponent (GvpA in GvpC), ki tvorijo stisljive plinske mehurčke, smo povečali občutljivost sesalskih celic na ultrazvok in mehanske dražljaje.
- Po meri narejena naprava za generiranje ultrazvoka za stimulacijo sesalskih celic.
- V sesalskih celicah smo izrazili mehanosenzitiven senzor, ki je občutljiv na povišano koncentracijo kalcija in omogoča hitro celično reakcijo z oddajanjem svetlobe ob vzdraženju z dotikom ali ultrazvokom. Opisani senzor smo izkoristili tudi za risanje po celicah.
- Ciklično luciferazo, ki se aktivira ob proteolitični cepitvi, smo preizkusili, opisali in vključili v zbirko iGEM.
- Oblikovali smo set štirih ortogonalnih mestno specifičnih proteaz, ki smo jih preizkusili kot cepljene proteine v sesalskih celicah.
- Oblikovali smo signalno pot na osnovi ortogonalnih proteaz, ki nam hkrati omogoča procesiranje več vhodnih signalov in jo ekperimentalno preizksuili.
- Proteoliza sekvence, ki omogoča zadrževanje proteina v endoplazemskem retiklu smo uporabili za sprožitev izločanja proteinov iz celic, kar je potrebno za hitre terapevtske odzive, kot na primer sproščanje hormonov ali nevroaktivnih peptidov.



